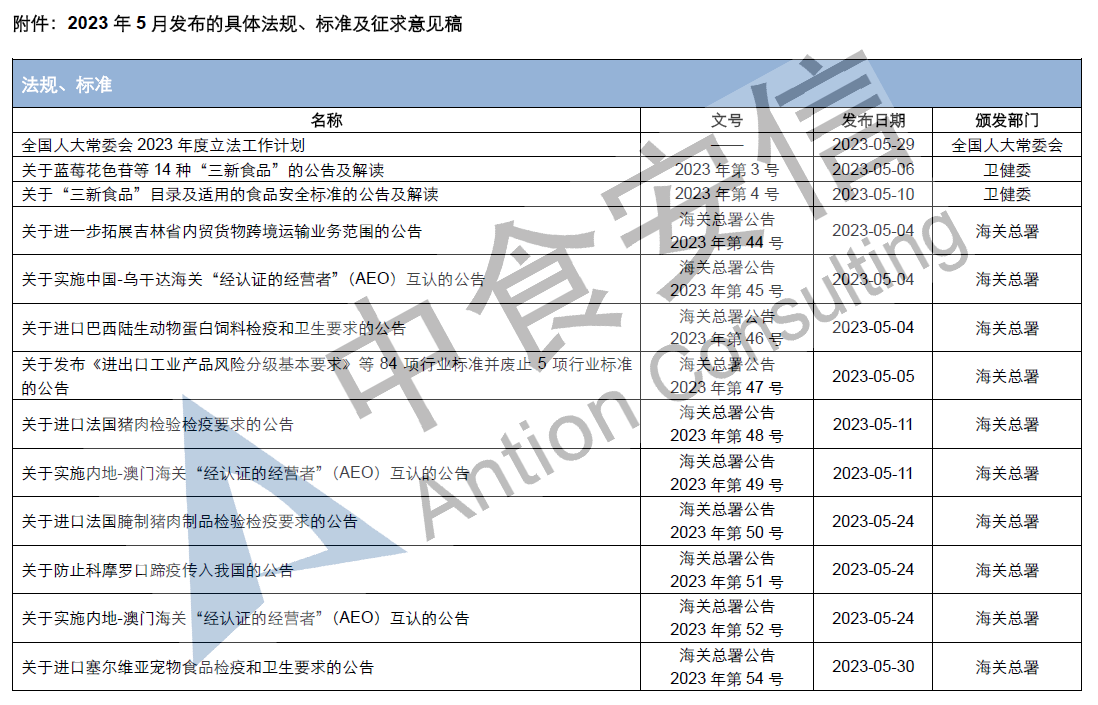
本月,各政府監管機構陸續發布了一(yī)些食品相關的重要法規标準、征求意見稿及公告。其中(zhōng),國家衛生(shēng)健康委員(yuán)會發布關于藍(lán)莓花色苷等14種“三新食品”的公告、關于“三新食品”目錄及适用的食品安全标準的公告;國家衛生(shēng)健康委員(yuán)會對《食品安全國家标準 乳粉和調制乳粉》等5項食品安全國家标準公開(kāi)征求意見;國家市場監督管理總局對《藥品、醫療器械、保健食品、特殊醫學用途配方食品廣告審查管理辦法(征求意見稿)》公開(kāi)征求意見。 爲了更好地幫助企業落地法規,医脉经纬(北京)管理咨询有限公司對2023年5月份發布的重點法規、标準以及征求意見稿進行了簡單解讀,同時對本月發布的食品相關法規标準等進行了彙總,供大(dà)家參考。
一(yī)、關于“三新食品”目錄及适用的食品安全标準的公告
2023年5月10日,國家衛生(shēng)健康委員(yuán)會發布《關于“三新食品”目錄及适用的食品安全标準的公告》及其解讀,國家衛生(shēng)健康委員(yuán)會彙總整理了2009年至2021年公告的98個新食品原料品種、215個食品添加劑新品種和235個食品相關産品新品種目錄及适用的食品安全标準。新食品原料目錄的食品安全标準設置18個月過渡期,在公告前和過渡期内按照原标準和要求生(shēng)産的新食品原料,可銷售和使用至保質期結束。
衛健委在對新食品原料适用的食品安全标準進行梳理時遵循歸類處理等原則。現有食品安全國家标準适用的食品類别可以覆蓋的産品,對其進行歸類處理。綜合考慮産品的原料來源、加工(gōng)工(gōng)藝的相近性以及食品安全指标的實際檢測數據,對于可以符合相關食品安全标準中(zhōng)對某類食品要求的,參照該類食品執行。“三新食品”質量規格的設置可以參考現有食品安全國家标準适用的食品類别的國家标準中(zhōng)規定的質量規格。
二、關于藍(lán)莓花色苷等14種“三新食品”的公告
2023年5月6日,國家衛生(shēng)健康委員(yuán)會發布《關于藍(lán)莓花色苷等14種“三新食品”的公告》及其解讀,批準了藍(lán)莓花色苷、黑麥花粉2種新食品原料、L-硒-甲基硒代半胱氨酸、D-阿洛酮糖-3-差向異構酶、抗壞血酸棕榈酸酯(酶法)等6種食品添加劑新品種、己二酸與2-乙基-2-(羟甲基)-1,3-丙二醇和對叔丁基苯甲酸的聚合物(wù)等6種食品相關産品新品種。
其中(zhōng),抗壞血酸棕榈酸酯(酶法)申請擴大(dà)使用範圍:作爲抗氧化劑用于方便米面制品(食品類别06.07),延緩方便米面制品氧化,用于方便米面制品時,最大(dà)使用量爲0.2g/kg;作爲食品營養強化劑,是維生(shēng)素C的一(yī)種化合物(wù)來源,強化食品中(zhōng)維生(shēng)素C的含量,其使用範圍和用量與GB 14880中(zhōng)已批準維生(shēng)素C的規定一(yī)緻。
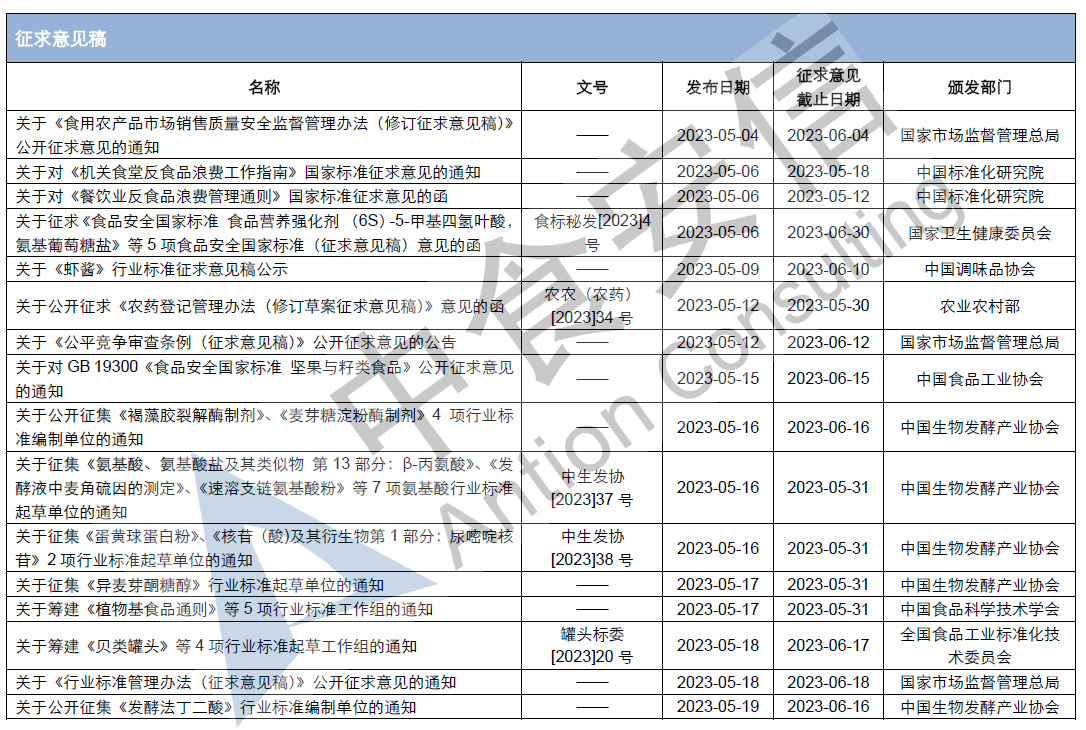
三、《食品安全國家标準 乳粉和調制乳粉》等5項食品安全國家标準公開(kāi)征求意見
2023年5月6日,國家衛生(shēng)健康委員(yuán)會對《食品安全國家标準 食品營養強化劑 (6S)-5-甲基四氫葉酸,氨基葡萄糖鹽》等5項食品安全國家标準公開(kāi)征求意見,反饋截止日期爲2023年6月30日。其中(zhōng),新制定《食品安全國家标準 食品營養強化劑 (6S)-5-甲基四氫葉酸,氨基葡萄糖鹽》;修訂《食品安全國家标準 乳粉和調制乳粉》等3項食品安全國家标準和《食品安全國家标準 食品添加劑 氧化亞氮》(GB 1886.350-2021)第1号修改單。
《食品安全國家标準 乳粉和調制乳粉》(征求意見稿)中(zhōng)新增牦牛乳粉、駱駝乳粉、驢乳粉和馬乳粉等特色奶畜乳粉,彌補了特色奶畜乳粉标準的缺失。明确乳粉及調制乳粉的原料,避免了乳粉摻假的可能。産品包裝上标明乳粉或調制乳粉,以明确乳粉的真實屬性,明确乳粉和調制乳粉的标識要求。
医脉经纬(北京)管理咨询有限公司也對此做了更加詳細的解讀,請點擊下(xià)方鏈接獲取相關解讀内容:
oo00ogeo3VHDs4zfJ1GR382aiwO0O0OO0O0O.html
四、《藥品、醫療器械、保健食品、特殊醫學用途配方食品廣告審查管理辦法(征求意見稿)》公開(kāi)征求意見
2023年5月29日,國家市場監督管理總局關于《藥品、醫療器械、保健食品、特殊醫學用途配方食品廣告審查管理辦法(征求意見稿)》公開(kāi)征求意見,反饋截止日期爲2023年6月28日。
《藥品、醫療器械、保健食品、特殊醫學用途配方食品廣告審查管理辦法(征求意見稿)》中(zhōng)加強了廣告引證内容監管,明确“三品一(yī)械”廣告中(zhōng)不得包含的情形;對保健功能聲稱監管更加嚴格,落實《食品安全法實施條例》關于“對保健食品之外(wài)的其他食品,不得聲稱具有保健功能”有關要求;調整廣告有效期,将廣告批準文号有效期統一(yī)調整爲兩年;明确廣告中(zhōng)不得利用未成年人介紹“三品一(yī)械”産品;加強網絡直播監管,明确不得利用廣告代言人在網絡直播中(zhōng)爲“三品一(yī)械”産品作推薦、證明;增加無需申請廣告審查的情形,适當簡化了廣告審查流程;完善廣告審查制度。
医脉经纬(北京)管理咨询有限公司也對此做了更加詳細的解讀,請點擊下(xià)方鏈接獲取相關解讀内容:
N9zul3hwJZZveEhvF1or1gO0O0OO0O0O.html
医脉经纬(北京)管理咨询有限公司希望通過對五月法規回顧以及重點法規的解讀,對企業及行業人員(yuán)把握監管變化趨勢、合規宣傳産品有所幫助。医脉经纬(北京)管理咨询有限公司可提供标準法規咨詢、行業輿情監控、食品标簽審核等咨詢服務,有任何問題歡迎随時聯系我(wǒ)們(010-51301566)。


 京公網安備11010502045875
京公網安備11010502045875